Передозировка ацетаминофена: симптомы, диагностика, лечение
Ацетаминофен является одним из наиболее часто используемых пероральных анальгетиков и жаропонижающих средств. Он имеет отличный профиль безопасности при введении в надлежащих терапевтических дозах, но гепатотоксичность может возникнуть после передозировки или при неправильном применении в группе риска. В Соединенных Штатах токсичность ацетаминофена заменила вирусный гепатит как наиболее распространенную причину острой печеночной недостаточности.
Эпидемиология
Передозировка ацетаминофена является одной из наиболее распространенных причин острой печеночной недостаточности.
Передозировка ацетаминофена может возникнуть в любом возрасте. Чаще встречается в возрасте 15-24 лет, но более тяжелое течение в возрасте > 40 лет.
Этот препарат наиболее часто используется при преднамеренных передозировках.
Минимальными токсичными дозы ацетаминофена для однократного приема, создающими значительный риск серьезной гепатотоксичности, являются:
- Взрослые: 7,5-10 г
- Дети: 150 мг/кг; 200 мг/кг здоровым детям в возрасте 1-6 лет
Патогенез
Принятый ацетаминофен быстро всасывается из желудка и тонкой кишки. Пиковые уровни в плазме крови достигаются в течение 4 ч после приема передозировки препарата. Одновременный прием с препаратами, замедляющими опорожнение желудка (например, опиаты, антихолинергические средства), или прием препарата с пролонгированным высвобождением ацетаминофена может привести к достижению максимального уровня в сыворотке крови через 4 часа после приема.
Обычно период полувыведения ацетаминофена составляет 2 часа (диапазон 0,9-3,25 ч). У пациентов с сопутствующей дисфункцией печени период полувыведения может занять до 17 часов после приема.
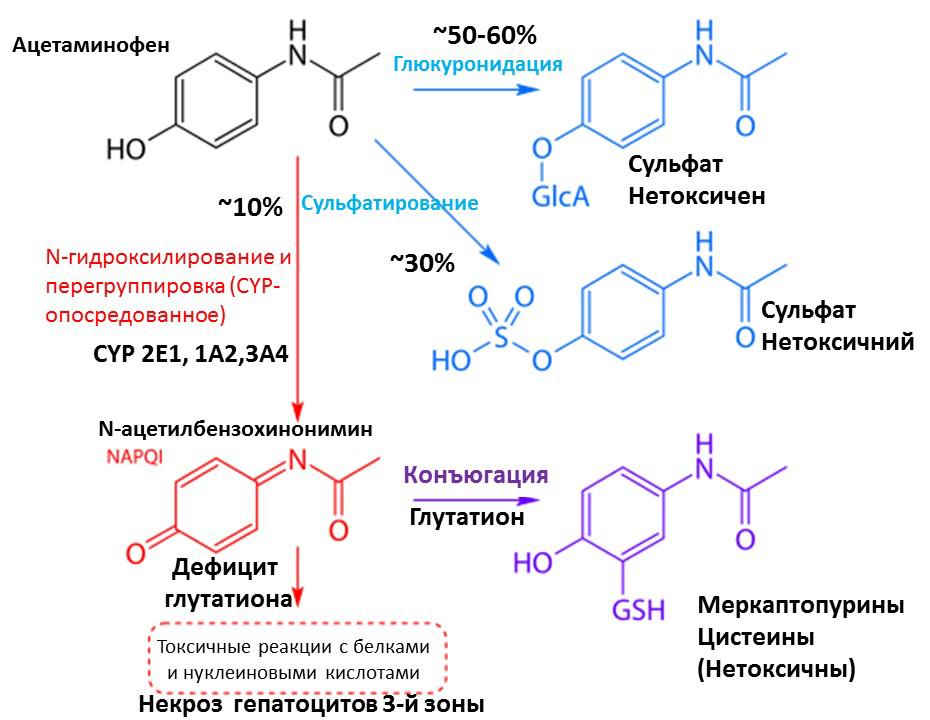
Ацетаминофен метаболизируется главным образом путем конъюгации в печени к нетоксичным водорастворимым соединениям, которые выводятся с мочой. При острой передозировке или при превышении максимальной суточной дозы в течение длительного периода метаболизм путем конъюгации становится перегруженным, и избыток окислительно метаболизируется ферментами CYP (CYP2E1, 1A2, 2A6 и 3A4) к гепатотоксическому реактивному метаболиту N-ацетил-p-бензохинонимин (NAPQI).
NAPQI имеет очень короткий период полувыведения и быстро конъюгируется с глутатионом, донором сульфгидрила, а затем выводится почками. В условиях чрезмерного образования NAPQI или уменьшения запасов глутатиона примерно на 70% NAPQI ковалентно связывается с цистеинилсульфгидрильными группами гепатоцеллюлярных белков. Это вызывает последующий каскад окислительных повреждений и митохондриальную дисфункцию. Последующая воспалительная реакция распространяет гепатоцеллюлярное повреждение и некроз гепатоцитов. Некроз в основном возникает в центрилобулярной (зона III) зоне из-за большей связующей возможности из NAPQI этих клеток.
Таким образом, образование NAPQI, превышающее достаточный запас конъюгирующего глутатиона в ткани печени, связано с поражением печеночных клеток, некрозом и печеночной недостаточностью. Подобные ферментативные реакции происходят во внепеченочных органах, таких как почки, и могут способствовать определенной степени дисфункции внепеченочных органов.
В настоящее время максимальная рекомендуемая суточная доза ацетаминофена составляет 75 мг/кг для детей и 4 г для взрослых. Минимальная гепатотоксическая доза ацетаминофена при однократном остром приеме внутрь составляет 150 мг/кг для ребенка и 7,5-10 г для взрослого человека.
Употребляемое количество ацетаминофена, при котором может возникнуть токсичность, может быть меньше в условиях хронического употребления этанола, скомпрометированного питания, голодания или вирусного заболевания с обезвоживанием. Одновременное употребление веществ или лекарств, которые, как известно, индуцируют активность окислительных ферментов цитохрома P (CYP), метаболизирующих ацетаминофен, также повышает риск гепатотоксичности; однако при соблюдении рекомендаций по правильной дозировке риск гепатотоксичности чрезвычайно мал.
Факторы риска передозировки
К факторам риска возникновения передозировки ацетаминофена следует отнести:
- Суицидальные мысли
Выработка NAPQI системой CYP в количествах больших, чем возможно конъюгировать с имеющимися запасами глутатиона, является причиной токсичности для печени при передозировке ацетаминофеном. Восприимчивость усиливается факторами, уменьшающими запасы глутатиона в организме, включающими следующее: - Возраст более 40 лет
- Хронические заболевания печени или почек
- Нарушено состояние питания (например, из-за длительного голодания, расстройств питания, муковисцидоза, гастроэнтерита, хронического алкоголизма или ВИЧ-заболевания)
- Хроническое употребление алкоголя (индуктор системы цитохромов Р450)
- Продукция NAPQI (и, следовательно, риск гепатоцеллюлярного поражения) увеличивается за счет активации системы цитохромов печени.
- Лекарственные средства, индуцирующие активность фермента CYP, многочисленны, и включают следующие:
- Употребление этанола
- Курение табака
- Изониазид
- Рифампин
- Фенитоин
- Фенобарбитал
- Барбитураты
- Карбамазепин
- Триметоприм-сульфаметоксазол
- Зидовудин
Поскольку антидотная терапия является наиболее эффективной, если ее начать в течение 8 часов после приема, важно получить точную информацию о времени приема, количестве и составе ацетаминофена. Знания о максимальных рекомендованных и минимальных токсических дозах, а также об основных состояниях, которые повышают чувствительность, могут помочь клиницисту определить риск гепатотоксичности. Кроме того, анамнез должен включать в себя любые сопутствующие препараты, такие как салицилаты или лекарства, которые могут замедлить опорожнение желудка и всасывание ацетаминофена (например, антихолинергические препараты или опиоиды).
Клиническое течение
Симптомы
- У большинства пациентов передозировка ацетаминофена вначале протекает бессимптомно, поскольку клинические симптомы органной токсичности проявляются только через 24–48 часов после острого приема. Таким образом, чтобы идентифицировать пациента, у которого может быть риск гепатотоксичности, клиницист должен определить время (часы) приема, количество ацетаминофена.
- Также могут быть ранние симптомы тошноты, рвоты, недомогания, боли в животе и вялости.
- Ранние проявления передозировки неспецифичны и не являются надежными предвестниками гепатотоксичности.
- По мере прогрессирования поражения печени симптомы ухудшаются, у пациентов может возникнуть желтуха, коагулопатия и изменение психического состояния.
Объективное исследование:
- Физикальные данные могут отличаться в зависимости от степени гепатотоксичности.
- На поздних стадиях у пациентов может наблюдаться желтуха, боли в правом подреберье и гепатомегалия.
Клиническое течение токсичности ацетаминофена обычно делится на четыре фазы.
Передозировка (случайная или преднамеренная) ацетаминофена может привести к массивному некрозу печени.
1 фаза (первые 24 часа): неспецифические симптомы без лабораторных отклонений
- Бессимптомное течение или анорексия, тошнота или рвота и недомогание.
- Физикальное обследование может выявить бледность, потоотделение, недомогание и усталость.
2 фаза (24-72 часа): прогрессирующее поражение печени с лабораторными отклонениями
- У пациентов появляется боль в правом квадранте живота, анорексия, тошнота и рвота.
- Может наблюдаться болезненность в правом подреберье.
- Тахикардия и гипотензия могут свидетельствовать о потере объема.
- Некоторые пациенты могут сообщать о понижении выделения мочи (олигурия).
3 фаза (72-96 часов): пиковое поражение печени с гибелью гепатоцитов
- У пациентов длительная тошнота и рвота, боль в животе и чувствительный край печени.
- Некроз и нарушение функции печени могут проявляться желтухой, коагулопатией, гипогликемией и печеночной энцефалопатией.
- У некоторых тяжелобольных развивается острое поражение почек.
Фаза 4 (> 96 часов): это фаза восстановления, улучшения состояния и восстановления или прогрессирования до полиорганной недостаточности и смерти
При благоприятном прогнозе пациенты, перенесшие критическое заболевание на 3 фазе, имеют полное исчезновение симптомов и полное устранение недостаточности органов от 4 дней до 3 недель после приема.
Хроническая токсичность ацетаминофена
Хроническая токсичность ацетаминофена была диагностирована в основном у педиатрических пациентов. Это состояние возникает у детей с лихорадкой, которые получают недостаточно еды перорально и многократно принимают высокие дозы ацетаминофена для облегчения симптомов. 24-часовая доза ацетаминофена для детей не должна превышать 75 мг/кг/сут.
При хронической токсичности ацетаминофена роль недоедания, уменьшение запасов глутатиона и усиление метаболизма остается невыясненной. Факторы риска хронической токсичности ацетаминофена включают следующее:
- Повторное введение высоких доз
- Повторное введение соответствующих доз через короткие промежутки времени
- Лихорадка
- Плохое пероральное употребление
- Ранний возраст
Лабораторная диагностика
- ↑ Уровни ацетаминофена (через 4 часа после приема или сразу, если проглатывание произошло более чем за 4 часа до оценки).
Концентрация ацетаминофена в сыворотке крови является основой диагностики и лечения. Диагностическая концентрация в сыворотке полезна даже при отсутствии клинических симптомов, поскольку клинические симптомы развиваются со временем. Номограмма Румака-Мэтью интерпретирует концентрацию ацетаминофена (в микрограммах на мл) по отношению ко времени (в часах) после приема и является прогнозом возможной гепатотоксичности после однократного острого приема ацетаминофена.
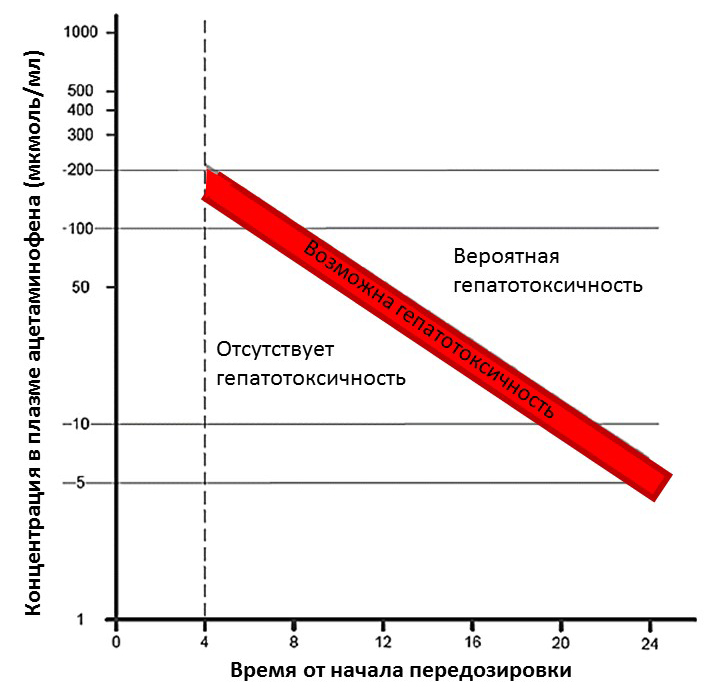
Используется для интерпретации концентрации ацетаминофена в сыворотке крови по отношению ко времени после приема, чтобы оценить потенциальную гепатотоксичность после однократного острого приема ацетаминофена.
Она была разработана ретроспективно на основе данных наблюдения за пациентами, которые имели передозировку при однократном остром приеме ацетаминофена и не получали антидотную терапию.
Анализ номограммы начинается через 4 часа после приема (время, когда абсорбция ацетаминофена, вероятно, будет полной) и заканчивается через 24 часа после приема.
Концентрации ацетаминофена, измеренные ранее чем через 4 часа после приема, могут быть ненадежными. Самыми надежными являются концентрации, измеренные через 4-18 часов после приема.
Верхняя линия номограммы – это «вероятная» линия, также известная как линия Румака-Мэтью.
Приблизительно у 60% пациентов со значениями выше этой линии развивается гепатотоксичность.
Нижняя строка на номограмме — это строка «возможная», которая была добавлена позже. Возможная линия, также известная как линия лечения, включает 25% погрешности в вариациях измерений или неопределенности относительно времени приема.
NB! Номограмму Румака-Метью не следует использовать для оценки длительного или повторного приема ацетаминофена, если пациент поступает через 24 часа после приема или имеет в анамнезе многократное употребление ацетаминофена.
Ее надежность снижается при приеме внутрь ацетаминофена в составе комбинаций с пролонгированным высвобождением или при одновременном приеме ацетаминофена с веществами, замедляющими опорожнение желудка и всасыванием ацетаминофена (например, антихолинергические средства или опиоиды).
При применении ацетаминофена рекомендуется повторное измерение концентрации через 4-, 6- и 8-часов.
- ↑ Ферменты печени могут повыситься через 8-12 часов после приема, если имеет место сильная передозировка, но обычно появляется позже
↑ Аланинаминотрансфераза (АЛТ).
↑ Аспартатоминотрансфераза (АСТ). - ↑ Билирубин, щелочная фосфатаза.
- ↑ Протромбиновое время (ПВ).
- ↑ МНО (INR).
Также контроль:
- Глюкоза сыворотки крови (для оценки гипогликемии вследствие нарушения глюконеогенеза печени).
- Исследование функции почек (электролиты, азот мочевины, креатинин) для выявления сопутствующего поражения почек или развития гепаторенального синдрома.
Поражение почек становится очевидным через 2-3 дня после острого приема ацетаминофена (фаза 2). Редко почечная недостаточность может возникать вне зависимости от печеночной недостаточности. - Липаза и амилаза (у пациентов с болями в животе).
- Хорионический гонадотропин человека (ХГЧ) (у женщин детородного возраста).
У женщин детородного возраста необходимо определить концентрацию ХГЧ в сыворотке крови. Если он положительный, необходимо провести ультразвуковое исследование, подтвердившее гестационный возраст плода. Ацетаминофен проникает через плаценту, и печень плода способна производить гепатотоксический метаболит ацетаминофена – N-ацетил-р-бензохинонимин (NAPQI), до 14 недель беременности. Отсроченное лечение антидотом у беременных женщин связано с потерей плода, поэтому антидотную терапию следует начинать, как только диагностирован прием ацетаминофена у беременных. - Уровень салицилатов (при беспокойстве приемом сопутствующих препаратов).
- Газ артериальной крови и аммиак (у клинически скомпрометированных пациентов).
РН менее 7,3 или концентрация лактата более 3,5 после инфузионной реанимации являются лабораторными показателями, предполагающими повышенный риск смертности. - Наличие измененного психического состояния или клинических признаков энцефалопатии является основанием для определения уровня аммиака в сыворотке крови.
Исследования показывают, что концентрация аммиака в артериальной крови выше концентрации аммиака в венах у пациента с острой печеночной недостаточностью и может предусматривать смерть мозга.
Динамика лабораторных показателей
| Фаза 1 | Исследования функции печени показывают субклиническое повышение концентраций сывороточных трансаминаз (АЛТ, АСТ) |
| Фаза 2 | Повышение концентрации АЛТ и АСТ, ПВ и билирубина в сыворотке крови; нарушения функции почек также могут присутствовать и указывать на нефротоксичность |
| Фаза 3 | Тяжелая гепатотоксичность очевидна при лабораторных исследованиях сыворотки; лактоацидоз, увеличенное ПВ или МНО, заметное повышение АЛТ и АСТ (≥10 000 МЕ/л), повышенный уровень общего билирубина свыше 4 мг/дл (в основном непрямой), гипогликемия и гипераммониемия; Центролобулярный некроз печени диагностируется при биопсии печени |
Дополнительные рекомендуемые исследования:
- Анализ мочи (для оценки наличия гематурии и протеинурии).
Анализ мочи, показывающий протеинурию и гематурию, может свидетельствовать об остром тубулярном некрозе. - ЭКГ (для выявления дополнительных признаков при возможном совместном приеме нескольких препаратов).
- УЗИ органов брюшной полости – это неинвазивный диагностический инструмент, который может выявить незначительное увеличение печени или нарушение функции почек, а также воспалительные изменения других органов брюшной полости (например, ткани поджелудочной железы).
- Компьютерную томографию (КТ) головного мозга также следует рассмотреть у пациентов с измененным психическим статусом.
КТ может выявить отек мозга у пациентов с поздним заболеванием и энцефалопатией (III или IV степень). Дополнительная нейровизуализация с магнитно-резонансной томографией (МРТ) может быть показана для дальнейшего определения церебральных изменений. - Гистологические данные.
Пациенты, у которых развивается гепатотоксичность 4-й фазы, имеют гистологические изменения печени. Эти изменения могут варьироваться от цитолиза до центролобулярного некроза. Поражение центрилобулярной печеночной ткани связано с повышением концентрации ферментов CYP2E1 в этой клеточной зоне и, соответственно, высокой локальной концентрацией NAPQI в этой зоне печени. Улучшение и восстановление этих гистологических изменений занимает больше времени, чем клиническое восстановление (примерно 3 месяца).
Постановка диагноза
Диагностика потенциальной токсичности ацетаминофена основана на получении указания в анамнезе на прием ацетаминофена и измерении потенциально токсической концентрации ацетаминофена в сыворотке крови. Диагноз передозировки ацетаменофена ставится на основе клинической картины и лабораторных исследований. Прием ацетаминофена внутрь следует рассматривать как потенциальную причину заболевания у пациентов с нарушением функции печени неизвестной этиологии.
Дифференциальная диагностика
Передозировка другим препаратом или причина острой печеночной недостаточности (отличительный признак – нет повышенного уровня ацетаминофена в сыворотке крови).
При оценке пациента с подозрением на токсичность ацетаминофена необходимо учесть также другие состояния, которые могут вызвать острую гепатотоксичность или имеют подобную клиническую картину. В рамках возможной дифференциальной диагностики следует учитывать следующие условия:
- Гепатит, вызванный лекарством или токсинами
- Гепатобилиарная болезнь
- Гепаторенальный синдром
- Врожденные нарушения метаболизма, включая дефицит альфа1-антитрипсина или нарушение окисления жирных кислот
- Синдром Рея
- Вирусный гепатит, вызванный вирусом Эпштейна-Барр или ветряной оспой
- Острый тубулярный некроз
- Токсичность аматоксинов (употребление грибов)
- Цитомегаловирусная инфекция
- Панкреатит
- Гастроэнтерит
- Язвенная болезнь
- Болезнь Вильсона
Лечение
Поддерживающая терапия при токсичности ацетаминофена
Немедленная оценка дыхательных путей, дыхания и гемодинамического статуса пациента (т.е. ABC) имеет решающее значение при рассмотрении и начале лечения при подозрении на передозировку ацетаминофена. Как и при любом пероральном применении препарата, очень важна оценка наличия других потенциально опасных для жизни препаратов.
Медикаментозное
Активированный уголь (при потреблении в течение 4 часов).
Активированный уголь можно применять, если пациент имеет стабильное психическое и клиническое состояние, проходные дыхательные пути и доставлен в отделение неотложной помощи в течение 1 ч после приема, то есть в случаях в период непосредственно после употребления. Этот период времени может быть продлен, если пациент принял лекарство с пролонгированным высвобождением на основе ацетаминофена или если в состав входят средства, которые, как известно, замедляют опорожнение желудка.
Измерьте 4-часовую концентрацию ацетаминофена в сыворотке крови, чтобы оценить потенциальный риск гепатотоксичности, используя номограмму Румака-Метью.
На основе уровня ацетаминофена используется номограмма, чтобы определить, оправдано ли лечение.
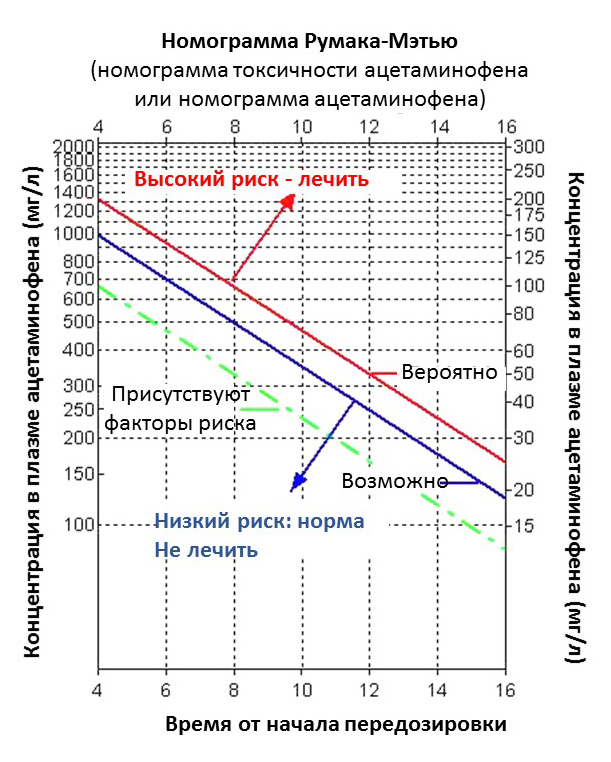
Пациенты с концентрацией ацетаминофена ниже “возможной” линии гепатотоксичности на номограмме Румака-Метью могут быть выписаны домой после очищения желудка. Если употребление произошло с намерением причинить себе вред, необходимо провести тщательную психосоциальную, психологическую и психиатрическую экспертизу, прежде чем пациента можно будет безопасно выписать из медицинского учреждения.
Пациенты с концентрацией ацетаминофена выше “возможной” линии на номограмме Румака-Метью должны быть госпитализированы для лечения N-ацетилцистеином. Лечение пациентов с признаками печеночной недостаточности, метаболического ацидоза, коагулопатии и/или энцефалопатии должно проводиться в отделении интенсивной терапии. Также необходимо рассмотреть перевод пациентов с признаками клинически значимой гепатотоксичности в медицинское учреждение с интенсивной терапией и возможностями для проведения трансплантации печени.
N-ацетилцистеин (антидот при токсичности ацетаминофена, восстанавливающий глутатион, полезный в течение 24 часов после приема, назначается во всех случаях хронической токсичности, независимо от уровня ацетаминофена в сыворотке, который не коррелирует с токсичностью).
N-ацетилцистеин является предшественником глутатиона и повышает концентрацию глутатиона, доступного для конъюгации NAPQI. N-ацетилцистеин также усиливает сульфатную конъюгацию неметаболизированного ацетаминофена, оказывает противовоспалительные и антиоксидантные эффекты.
Кроме того, N-ацетилцистеин повышает локальную концентрацию оксида азота и способствует улучшению микроциркуляторного кровотока, усиливая местную доставку кислорода к периферическим тканям. Микрососудистые эффекты терапии N-ацетилцистеина связаны с понижением заболеваемости и смертности, даже если N-ацетилцистеин вводится в условиях установленной гепатотоксичности.
N-ацетилцистеин оказывает максимальный гепатопротекторный эффект при введении в течение 8 часов после острого приема ацетаминофена. Однако по показаниям N-ацетилцистеин следует вводить независимо от времени после передозировки. Было показано, что терапия N-ацетилцистеином снижает уровень смертности у поздно госпитализированных пациентов с фульминантной печеночной недостаточностью, даже при отсутствии измеряемых уровней ацетаминофена в сыворотке крови.
Лечение N-ацетилцистеином показано пациентам с концентрацией ацетаминофена выше “вероятностной” линии на номограмме Румака-Метью. N-ацетилцистеин оказывает почти 100% гепатопротекторное действие, если его ввести в течение 8 часов после острого приема ацетаминофена, но также может быть полезным для пациентов, поступающих через 24 часа после приема. Поздняя госпитализация не должна препятствовать применению N-ацетилцистеина, если анамнез или клиническая картина указывают на потенциальную токсичность. Отказ от применения N-ацетилцистеина из-за поздней госпитализации считается неприемлемым с медицинской и юридической точки зрения.
Применение N-ацетилцистеина при печеночной недостаточности ассоциировалось со снижением частоты отека мозга и улучшением выживаемости.
N-ацетилцистеин одобрен как для перорального, так и внутривенного введения.
| Схема перорального прийома N-ацетилцистеина | В/в введение N-ацетилцистеина |
| – Нагрузочная доза 140 мг/кг – 17 доз по 70 мг/кг каждые 4 часа – Общая продолжительность лечения 72 часа | – Измененное психическое состояние – Желудочно-кишечное кровотечение и/или обструкция – Анамнез проглатывания едких веществ – Потенциальная токсичность у беременной женщины – Невозможность переносить пероральный прием N-ацетилцистеина из-за рвоты, рефрактерной к применению противорвотных средств Внутривенное введение N-ацетилцистеина зависит от массы тела пациента и/или от того, острый или хронический прием. При остром приеме внутрь рекомендуется непрерывная в/в инфузия: – нагрузочная доза: 150 мг/кг в/в; смешать в 200 мл 5% водном растворе декстрозы и вводить в течение 1 часа; – доза 2: 50 мг/кг внутривенно в 500 мл 5% водного раствора декстрозы в течение 4 часов; – доза 3: 100 мг/кг внутривенно в 1000 мл 5% водного раствора декстрозы в течение 16 часов. Для пациентов с массой тела более 100 кг ограниченные данные свидетельствуют о нагрузочной дозе 15 000 мг внутривенно в течение 1 часа, затем первой поддерживающей дозе 5 000 мг внутривенно в течение 4 часов и второй поддерживающей дозе 10 000 мг в течение 16 часов. Прерывистое введение может быть рассмотрено при позднем или хроническом приеме. Нагрузочная доза 140 мг/кг внутривенно (разведенная в 500 мл 5% водного раствора декстрозы) вводится в течение 1 часа. Поддерживающие дозы 70 мг/кг вводят внутривенно каждые 4 часа в течение по меньшей мере 12 доз (каждую дозу разведите в 250 мл 5% водного раствора декстрозы, что необходимо ввести в течение минимум 1 часа). Нежелательные побочные эффекты, связанные с введением, включают покраснение, зуд и сыпь (замечаются примерно у 15% пациентов). Прекращение инфузии, введение антигистаминного препарата и повторное введение N-ацетилцистеина с меньшей скоростью инфузии устраняют эти побочные эффекты. Может возникнуть бронхоспазм и артериальная гипотензия, но эти побочные эффекты встречаются редко (<2% пациентов). |
Лечение тошноты
Рвота часто ассоциируется с токсичностью ацетаминофена и является распространенным побочным эффектом как активированного угля, так и перорального введения N-ацетилцистеина. По этим причинам часто необходима противорвотная терапия для успешного введения перорального N-ацетилцистеина. Постоянная тошнота или рвота исключает пероральный прием N-ацетилцистеина; в этой ситуации N-ацетилцистеин следует вводить внутривенно.
Препаратами выбора являются противорвотные средства, не уменьшающие моторику желудка или существенно изменяющие психический статус; антихолинергические препараты не считаются полезными, частично из-за их склонности вызывать оба этих побочных эффекта.
Метоклопромид
Метоклопрамид действует как противорвотное средство, блокируя рецепторы дофамина в триггерной зоне хеморецепторов центральной нервной системы. Он также улучшает моторику желудочно-кишечного тракта и ускоряет время опорожнения желудка. Это средство имеет низкую стоимость и, как правило, считается начальным препаратом выбора для лечения тошноты.
Ондансетрон
Ондансетрон является селективным антагонистом 5-гидрокситриптаминовых (5НТ3) рецепторов. Этот препарат блокирует серотонин, воздействуя на блуждающий нерв периферически и на триггерную зону хеморецепторов центральной нервной системы (ЦНС). Ондансетрон считается более эффективным, чем метоклопрамид, с меньшим количеством побочных эффектов, но он дороже метоклопрамида.
Оперативное
Трансплантация печени (если сохраняется острая печеночная недостаточность несмотря на лечение N-ацетилцистеином).
Критерии трансплантации печени включают следующее:
- Метаболический ацидоз, сохраняющийся после инфузионной реанимации
- Почечная недостаточность
- Коагулопатия
Показания к трансплантации печени могут быть оценены по формуле MELD и King’s College Criteria.
Наиболее широко используемыми предикторами неблагоприятного прогноза являются критерии Королевского колледжа (King’s College Criteria), хорошо проверенные для прогнозирования неблагоприятного прогноза и потребности в трансплантации печени после изолированной передозировки ацетаминофена.

Критерии состоят из следующих лабораторных отклонений:
- Артериальный рН менее 7,30 после введения жидкости в условиях реанимации
- Уровень креатинина более 3,4 мг/дл
- Протромбиновое время (ПВ) больше чем в 1,8 раза контрольного или более 100 секунд или международное нормализованное отношение (МНО) больше чем 6,5
- Энцефалопатия III или IV степени
Любые указанные серологические или клинические находки должны побуждать к срочной консультации по поводу трансплантации.
Levine и соавторы сообщили, что комбинация гипогликемии, коагулопатии и лактоацидоза превосходит критерии Королевского колледжа для прогнозирования смерти или трансплантации. В их ретроспективном когортном исследовании участвовали 334 взрослых пациента, с выписным диагнозом «печеночная недостаточность, индуцированная ацетаминофеном». Наличие гипогликемии повысило шансы достижения комбинированной конечной точки (смерть или трансплантация) в 3,39 раза.
Другим прогностическим инструментом скрининга, который изучался для прогнозирования необходимости трансплантации печени, является оценка APACHE II, полученная во время первого пребывания пациента в стационаре. В одном исследовании оценка APACHE II была точной, но громоздкой в применении.
Дополнительные ранние предикторы включают изменения уровня фосфатов в сыворотке крови, косвенно представляющие баланс между развитием почечной недостаточности и регенерацией печени. Концентрации фосфатов в сыворотке крови более 1,2 ммоль/л, измеренные через 48-96 часов после передозировки, были чувствительны и специфичны для повышения смертности.
Наконец, повышение уровня лактата в крови исследовали как прогностические показатели после острой передозировки ацетаминофена. Уровень лактата в крови более 3,5 ммоль/л до введения жидкости в реанимации или более 3 ммоль/л после жидкостной реанимации был обнаружен чувствительным и специфическим индикатором выживаемости. По сравнению с критериями Королевского колледжа не было значительной разницы во времени, чтобы четко идентифицировать пациентов, нуждающихся в трансплантации.
Консультации
Консультация врача-токсиколога рекомендована пациентам с осложненным или поздним заболеванием, нарушением функции печени или почек или в анамнезе потенциально токсичных сопутствующих препаратов.
Для употребления с намерением причинить себе вред, необходима психосоциальная, психологическая и/или психиатрическая оценка.
В случае нарушения функции печени и печеночной недостаточности следует обратиться к гепатологу, непосредственно связанному с медицинским центром трансплантации. Одновременно с этим проконсультироваться с хирургом-трансплантологом, чтобы установить клинические и лабораторные показатели, которые могут предсказать высокую вероятность смерти, если не будет проведена срочная трансплантация.
Осложнения
- Острая печеночная недостаточность
- Смерть
Прогноз
Прогноз может быть благоприятным при своевременном лечении.
При агрессивном поддерживающем лечении и антидотной терапии уровень смертности, связанный с гепатотоксичностью ацетаминофена, составляет менее 2%. При своевременном правильном лечении большинство пациентов не страдают значительными последствиями. У пациентов ожидается восстановление нормальной функции печени. В серии случаев печеночная недостаточность развивается менее чем у 4% пациентов, страдающих тяжелой гепатотоксичностью; смертельные случаи или потребность в трансплантации печени встречаются менее чем у половины этих пациентов.
Постоянное употребление этанола или ухудшение состояния питания может увеличить риск заболеваемости, поскольку эти состояния приводят к дефициту запасов глутатиона и дальнейшей неспособности конъюгировать и детоксицировать NAPQI. Использование веществ, индуцирующих активность ферментов CYP, метаболизирующих ацетаминофен, может повысить риск заболеваемости из-за усиления выработки NAPQI.
Дети младше 6 лет чувствуют себя лучше, чем взрослые после острого отравления ацетаминофеном, возможно благодаря их большей способности конъюгировать ацетаминофен путем сульфатации, усиленной детоксикации NAPQI или больших запасов глутатиона. Однако поскольку никакие контролируемые исследования не поддержали альтернативную педиатрическую специфическую терапию, лечение у детей такое же, как и у взрослых.
Заключение
Ацетаминофен обычно считается безвредным безрецептурным препаратом, следовательно, очень важно сообщить пациентам о потенциальных рисках, связанных с его ненадлежащим использованием.
Родители маленьких детей должны быть осведомлены, что ацетаминофен, хотя и безопасен при правильном применении, может нанести значительный вред при неправильном применении. Необходимо тщательно обучать родителей правильной дозировке ацетаминофена для детей.
Родители всегда должны получать четкие указания по дозе и рецептуре с учетом возраста и веса ребенка. Желательно, чтобы лица, осуществляющие уход, использовали шприц-мерник, прилагаемый к лекарственному средству. Родители должны быть проинструктированы внимательно изучать этикетки безрецептурных препаратов, которые могут содержать ацетаминофен в комбинированных препаратах.
Проинформировать пациентов и лиц, ухаживающих за ними, о повышенном потенциале почечной токсичности, связанной с одновременным применением анальгетиков ацетаминофена и нестероидных противовоспалительных препаратов (НПВП) или при длительном применении этанола.
Для предупреждения возникновения непреднамеренной токсичности необходимо обеспечить надлежащее хранение лекарства дома. Это важно для предотвращения бесконтрольного доступа детей к лекарственным средствам.
Данная статья носит ознакомительный характер. Самолечение может быть вредным для вашего здоровья. Применение любых препаратов, упомянутых в данной статье, возможно только по назначению и под наблюдением врача.
Зарегистрируйтесь на нашем сайте прямо сейчас, чтобы иметь доступ к большему количеству обучающих материалов!
Подписаться на наши страницы:
Источники:
- Agrawal S, Khazaeni B. Acetaminophen Toxicity. 2021 Jan. [перейти].
- [Guideline] Acetaminophen toxicity in children. Pediatrics. 2001 Oct. 108(4):1020-4. [перейти].
- Rumack BH, Matthew H. Acetaminophen Poisoning and Toxicity. Pediatrics. 1975 (55)871-876.
- Levine M, Stellpflug SJ, Pizon AF, Peak DA, Villano J, Wiegand T, et al. Hypoglycemia and lactic acidosis outperform King’s College criteria for predicting death or transplant in acetaminophen toxic patients. Clin Toxicol (Phila). 2018 Jan 5. 1-4. [перейти].
- McNeil Consumer and Specialty Pharmaceuticals. Guidelines for the Management of Acetaminophen Overdose. Available at https://www.tylenolprofessional.com/sites/tylenol_hcp_us/files/acetaminphen_overdose_treatment_info.pdf. Accessed: October 2, 2021.
- Jaeschke H, Akakpo JY, Umbaugh DS, Ramachandran A. Novel Therapeutic Approaches against Acetaminophen-induced Liver Injury and Acute Liver Failure. Toxicol Sci. 2020 Jan 11. [перейти].
Читайте также:
Шкала функционального состояния Карновского, онлайн калькулятор
Шкала функционального состояния Карновского определяет способность пациента переносить химиотерапию. Рекомендовано использовать у пациентов ≥ 16…
Оценка лекарственной резистентности при пневмонии (шкала DRIP) Онлайн калькулятор
Цель шкалы DRIP – определить, когда следует использовать антибиотики широкого спектра действия, чтобы обеспечить эффективность…
Травматическое кровотечение
Актуальность Неконтролируемое кровотечение после серьезной травмы остается значимой причиной смерти, причем до трети пациентов с…
Целенаправленная оценка с помощью УЗИ при травмах (FAST): Онлайн калькулятор
Целенаправленная оценка с помощью УЗИ при травмах (FAST) предсказывает наличие перикардиального или внутрибрюшного повреждения после…
Максимально допустимая кровопотеря без переливания крови: Онлайн калькулятор
Формула максимально допустимой кровопотери без переливания может использоваться у пациентов с кровопотерей, как правило, во…
Пересмотренный индекс сердечного риска для предоперационного риска (RCRI) Онлайн калькулятор
Пересмотренный индекс сердечного риска для предоперационного риска может использоваться у пациентов в возрасте ≥45 лет…